中央ノルウェーでの野兎病のアウトブレイク 2011年1月~3月
Eurosurveillance 2011年03月31日
要約
2011年1月から3月まで、39例の野兎病がノルウェー中央部の3つの郡で診断されました。21例が口咽頭型で、10例がリンパ節型/潰瘍型。2例が肺炎型、2例が腸チフス型でした。3例は無症候性であり、臨床情報は1つの症例では入手できませんでした。平均年齢は40.3歳(範囲2歳から89歳)でした。34例は私設の井戸から飲料水を使用していたことが報告されました。げっ歯類(レミング)の増加と、雪解けによって、感染したげっ歯類やげっ歯類の排泄物による井戸の汚染が生じた可能性があります。
アウトブレイクについて
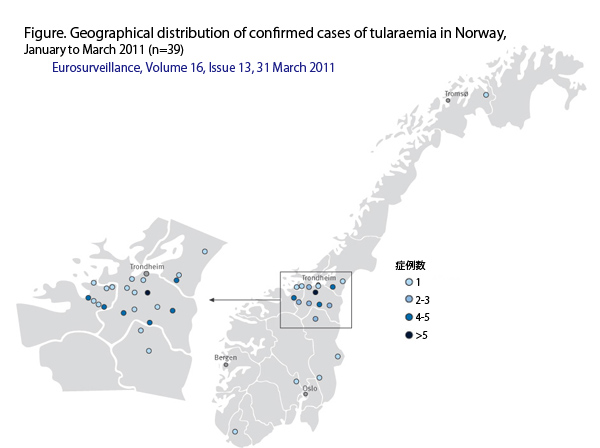
2011年1月1日から3月25日に、39例の野兎病確定症例(女性16例と男性23例)が、ノルウェー中央部のSør-Trøndelag(28例)、Møre og Romsdal(5例)、Nord-Trøndelag(6例)の3つの郡で報告されました。確定症例は野兎病の臨床症状に合致する症例、あるいは、前の症例と同じ水源から飲料水を使用しており、後述の方法で野兎病感染が実験室的に確認された例とされました。症例は、各郡の中に散在し、13の異なる市において生じていましたが、すべてに共通する感染源へのリンクは見られませんでした(図)。これと比較して、同じ時期にノルウェーでは、他の地域から合計7症例が報告されていました。2009年と2010年には、ノルウェー中央部からそれぞれ4症例と8症例が報告されました。
図2011年1月から3月にかけてのノルウェーの野兎病の確認症例地域分布(n=39)
野兎病は、細菌であるF.tularensisによって引き起こされる人獣共通感染症です。 F.tularensisには、tularensis、holarctica、mediasiatica、およびnovicida の4種類の亜種が知られています。ヨーロッパでの感染は、一般に亜種holarcticaによって生じ、北アメリカで一般的な亜種tularensisよりも症状が軽い傾向があります。いくつかの媒介動物がこの疾患の感染に関わっており、げっ歯類、および野兎などが一般的です。しかし、この感染症は虫に刺されることによっても感染する可能性があります[1]。
いくつかの臨床型が認められ、ノルウェーで最も一般的な臨床型は、口咽頭型およびリンパ節潰瘍型です[2]。口咽頭型は一般的に汚染された食品や水に関連して生じます。リンパ節潰瘍型は、感染動物との皮膚接触や、虫刺され後によく見られます[3]。
口咽頭型の野兎病のアウトブレイクは、以前に、いくつかの欧州諸国から報告されました[3,4]。野兎病はノルウェーでは届出伝染病で、過去10年間に3例のアウトブレイクが報告されました[5-7]。そして、そのすべてが死んだレミング(Lemmus lemmus)が以前にみられていた地域の水源と関連がありました。2001年から2010年まで、3例から66例の野兎病が、全国中で毎年報告され、平均症例は16例から32例まで増加しています(www.msis.noからデータが入手可能)。この増加は、上記のアウトブレイクで一部説明されるかもしれません。
診断と臨床像
ここで記述されているアウトブレイクに最も一般的な臨床像は、発熱と、咽頭炎(口咽頭型21例)と頸部リンパ節腫脹(リンパ節型/潰瘍型10例)でした。その他の8例の野兎病症例のうち2例は肺炎型と分類されました。そして、2例が腸チフス型として分類されました。3例は無症候性で、そして、1例では臨床情報が入手できませんでした。
診断は、30症例においては主として血清学的に(microagglutinationとin-house IgG/IgM Elisa法)[8]、また、7症例ではF.tularensis特異的なPCR分析で[9]、2症例では血液培養(BactAlert、BioMerieux)によって確定しました。この2例から分離された細菌はPCRによってF.tularensisであることが確認され、16S rDNA遺伝子配列が同定され、pdpAに対するPCRによって、亜種tularensisではないことが確認されています[10]。
39の診断症例のうち34症例は私設の井戸か川の水から飲料水をとっていました。PCRによって、F.tularensisDNAがSør-Trøndelagで検査された5か所の異なった井戸の濾過水から検出されました。1つの市の7症例が、同じ水源にリンクしていました。この事例を除いた2症例だけが、今までのところ共通の井戸を使用していたことが確認されています。いくつかの、感染源とのうわさのある水源に暴露を受けた人に対して、血清学的検査による追跡調査が推奨されています。
検討
現在のアウトブレイクは、ノルウェー中央部の3郡の多くの自治体に関わっています。口咽頭型の野兎病と、頸部リンパ節腫脹が、冬季に私設の井戸を使用したことにリンクして起きたという臨床像から、汚染された水がこのアウトブレイクの感染源として最も疑わしいと考えられます。いくつかの井戸でPCR分析によって、F.tularensisのDNAが検出されたことが、いくつかの症例に関しては前述の仮定を支持しています。正確なデータを得ることができませんが、私設井戸の使用はノルウェーの農村地域では比較的一般的なことです。
F.tularensisと井戸の汚染の間の正確なメカニズムは未知です。 しかしながら、2010年11月、12月は異常に寒い月が続き、その一方で、2011年1月には気温が上昇したため、融雪によってげっ歯類の死体やげっ歯類の排泄物によって汚染された表層水によって、私設井戸の汚染へとつながった可能性があります。野兎病の潜伏期は最大3週間あり、血清変換が生じるまで最大6週間かかる可能性があるため、より多くの症例が続いて生じる可能性があります。
野兎病は伝統的に「レミング熱」と「野兎ペスト」の両方の名前で呼ばれてきました。このことは、げっ歯類と野兎が病気を伝播していることを明確に示しています。げっ歯類の密度が大幅に増加する年は約3年から4年の間隔でみられ[11] 、ノルウェー南部および中央部では2010年の夏および秋に、レミングが多数みられたということです。同時に、ノルウェーの獣医学研究所はこれらの地域で広範囲にmountain hare(Lepus timidus)の野兎病がみられたことを観察しました[12]。mountain hareは、この感染に非常にかかりやすく、通常、暴露を受けてから数日以内に敗血症で死にます。
小川や私設の井戸を飲料水の水源として、また、その他の目的で使用していることは、ノルウェーの農村地域で懸念すべき問題です。国立公衆衛生院によって発行された既存ガイドラインでは、地域住民に対して、水系感染した野兎病が疑われた場合、あるいは確認症例がみられた場合には、飲料水を沸騰させること、および、死んだげっ歯類がいないかどうか井戸を点検するように助言しています。井戸の所有者はすべて、小げっ歯類が井戸に入るのを避けるために、あらゆる開口部を慎重に覆い、げっ歯類が入ることができるわずかな隙間も塞ぐように必要な努力をすべきです。また、雪解けの後に、井戸が表層水で汚染されないようにするのも重要です。井戸が汚染されたことが疑われた場合、その後、水を使用する前には消毒すべきです。しかし、小川から飲料水を得ている人の場合には、これは可能でないかもしれません。最近、ノルウェーの食品安全当局は、現在のアウトブレイクに関連して、同様のアドバイスと情報をメディア向けに、また、大衆向けに発表しました。各自治体の地域保健当局は、一般大衆に対するアドバイスや疑いのある飲料水の水源調査など、感染制御措置を講じる責任を負っています。
Eurosurveillance, Volume16, Issue13, 31 March 2011
参考文献
- 1.World Health Organization(WHO)Epidemic and Pandemic Alert and Response.WHO guidelines on tularaemia. Geneva:WHO; 2007.
http://www.who.int/csr/resources/publications/WHO_CDS_EPR_2007_7.pdf[PDF形式:1260KB] - 2.Brantsaeter AB. Twenty-five years of tularaemia in Norway, 1978–2002.Abstract number: 10.1111/j.1198-743X.2004.902_o142.x.European Society of Clinical Microbiology and Infectious Diseases. 14th European Congress of Clinical Microbiology and Infectious Diseases. Prague; 1-4 May 2004.
- 3.Tärnvik A, Priebe HS, Grunow R.Tularaemia in Europe:an epidemiological overview.Scand J Infect Dis. 2004;36(5):350-5.
- 4.Willke A, Meric M, Grunow R, Sayan M, Finke EJ, Splettstösser W, et al.An outbreak of oropharyngeal tularaemia linked to natural spring water.J Med Microbiol. 2009;58(Pt 1):112-6.
- 5.Rike HF, Vigerust A, Bergh K. Vannbårent utbrudd av tularemia(harepest)i Midtre Gauldal. [A waterborne outbreak of tularaemia in Midtre-Gauldal].Norwegian Institute of Public Health. 27 Oct 2003.Norwegian.
http://www.fhi.no/eway/default.aspx?pid=233&trg=MainLeft_5669&MainLeft_5669=5544:27208::0:5667:1:::0:0 - 6.Brantsaeter AB, Krogh T, Radtke A, Nygard K.Tularaemia outbreak in northern Norway.Euro Surveill. 2007;12(13):pii=3165.
http://www.eurosurveillance.org/ViewArticle.aspx?ArticleId=3165 - 7.Melien P, Holsdal RE.Tularemi i Meldal–en vanskelig diagnose? [Tularaemia in Meldal- a difficult diagnosis?].Norwegian Institute of Public Health. 18 Mar 2008.Norwegian.
http://www.fhi.no/eway/default.aspx?pid=233&trg=Area_5626&MainArea_5661=5619:0:15,4427:1:0:0:::0:0&MainLeft_5619=5626:68396::1:5625:1:::0:0&Area_5626=5544:68400::1:5628:1:::0:0 - 8.Bevanger L, Maeland JA, Naess AI.Competitive enzyme immunoassay for antibodies to a43,000-molecular-weight Francisella tularensis outer membrane protein in the diagnosis of tularemia.J Clin Microbiol. 1989;27(5):922-6.
- 9.Sjöstedt A, Erikson U, Berglund L, Tärnvik A.Detection of Francisella tularensis in ulcers of patients with tularaemia by PCR.J Clin Microbiol. 1997;35(5):1045-8.
- 10.Tomaso H, Scholz HC, Neubauer H, Al Dahouk S, Seibold E, Landt O, et al. Real-time PCR using hybridization probes for the rapid and specific identification of Francisella tularensis subspecies tularensis.Mol Cell Probes. 2007;21(1):12-6.
- 11.Semb-Johaansson A, Ims RA. Smågnagerne [Rodents]. Semb-Johansson A, Frislid R, editors. Oslo;1990. 121-71.Norwegian.
- 12.Norwegian Veterinary Institute.Flere tilfeller av harepest i Sør-Norge [Severeal cases of tularaemia in South-Norway].Norwegian Veterinary Institute. 25 Nov 2010.Norwegian.
http://www.vetinst.no/index.php/nor/Nyheter/Flere-tilfeller-av-harepest-i-Soer-Norge


